◆ 新薬情報 index
2014年7月製造販売承認
(印刷用画面へ)■アレセンサカプセル 20mg,40mg ■カナグル錠 100mg ■ザイティガ錠 250mg ■ジャカビ錠 5mg ■スンベプラカプセル 100mg ■ダクルインザ錠 60mg ■デルティバ錠 50mg ■ニシスタゴンカプセル 50mg,150m… ■ラパリムス錠 1mg ■スタレボ配合錠 L50,L100 ■アノーロエリプタ 7吸入用,30吸入用 ■クレナフィン爪外用液 10% ■ドボベット軟膏
■ ダクルインザ錠 60mg
|
|
| 1. 承認概要 | ||
| 新有効成分 2014年7月 / 2014年9月 発売 | ||
| 2. 薬効分類名 | ||
| 抗ウイルス剤/HCV NS3/4Aプロテアーゼ阻害剤 | ||
| 3. 一般的名称 | ||
| ダクラタスビル塩酸塩錠 | ||
| 4. 適応症 | ||
| セログループ1(ジェノタイプ1)のC型慢性肝炎またはC型代償性肝硬変におけるインターフェロンを含む治療法に不適格の未治療 あるいは不耐容の患者またはインターフェロンを含む治療法で無効となった患者のウイルス血症の改善 *2015年3月に、すべてのセログループ1のC型慢性肝炎、代償性肝硬変患者に対して承認され、使用可能となりました。 | ||
| 5. 類薬との比較 | ||
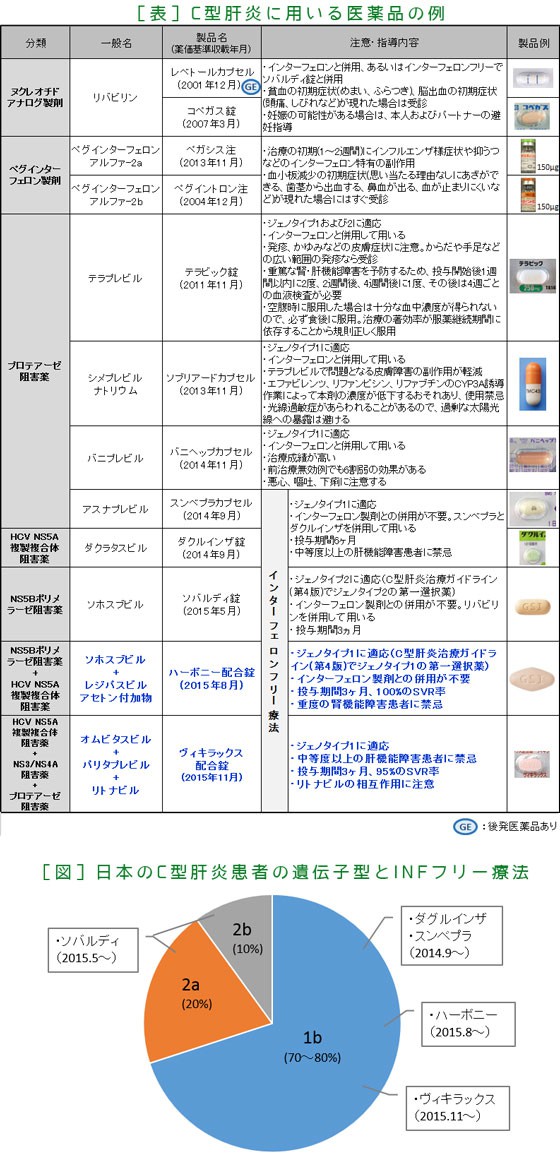 | ||
| 6. 特徴 | ||
| 【特徴】 インターフェロンを併用しない国内初の抗C型肝炎ウイルス薬で、スンベプラカプセルと併用して用います。 何らかの理由でインターフェロンを使えない患者か、過去に使って効果がなかった患者が適応となります。 また、現在ジェノタイプ1の標準治療であるシメプレビル(ソブリアード)を含む3 剤併用には代償性肝硬変の適応がありませんが、 この2剤併用は代償性肝硬変(Child-Pugh 分類A)にも使えます。 【作用機序】 ダクラタスビルと併用するアスナプレビルと共にC型肝炎ウイルス特有の分子を標的とする薬剤で、DAAs(Direct-acting Antiviral Agents:直接作用型抗ウイルス薬)と呼ばれています。 ダクラタスビル塩酸塩は、HCVの複製及び細胞内シグナル伝達経路の調節に関与するHCV NS5Aを強力かつ選択的に阻害します。 【背景】 肝癌が発症する原因のほとんどはウイルスによる慢性肝炎で、このうちC型肝炎が8割を占めます。 C型肝炎ウイルスは、遺伝子型によってタイプが異なります。 日本人患者の7割を占めるのが、インターフエロン製剤が効きにくいIb型(1型の一種)です。 近年、1型に高い有効率が示されたのが、2011年に承認されたプロテアーゼ阻害薬のテラブレビル(テラビック)で、 PEG-インターフェロン、リバビリン、およびテラブレビルを用いる3剤併用療法です。 この療法で治療成績が上がり、投与期間はこれまで1年間だったものが半年になりましたが、本剤は特に皮膚障害が問題となりました。 2013年に登場したのがシメプレビル(ソブリアード)で、皮膚障害が軽減されて使いやすくなり、本剤の登場によって治療ガイドラインも変更されました。 C型肝炎の治療では、長らくインターフェロンが中心に位置付けられてきました。 しかし、インターフェロンの投与には週1回の通院が必要となるほか、ほぼ全ての患者に何らかの副作用を生じます。 副作用が重篤な場合、投与量を減らしたり、治療を中断したりするため、決められた治療を完遂できないこともあります。 さらに、インターフェロンによる副作用から、治療を受けたくないという患者が少なくないため、本剤のようなインターフェロンフリーの治療を希望する患者も増えることが期待できます。 平成26年9月19日、肝炎治療特別促進事業において、「ダクラタスビル及び アスナプレビル併用療法」が追加されて、インターフェロンフリー2剤併用療法の医療費助成が開始されました。 なお、インターフェロンフリーの治療については、現在さらに複数の経口薬の開発が進められています。 【効果】 インターフェロンを併用する現在の標準治療に近い成績が得られています。 インターフェロンを含む治療法に不適格の未治療/不耐容患者(ジェノタイプ1bのC型慢性肝炎患者)に対するSVR24達成率1は87.4%、 前治療(IFN及びリバビリン併用)無効患者のSVR24達成率1は80.5%でした。 【副作用・課題】 主な副作用としては、肝機能障害があります。第3相試験では、ALT上昇が15.8%、AST上昇が12.6%に見られました。 このため、治療開始12週目までは少なくとも2週毎、それ以降は4週毎に肝機能検査が必要です。 経口薬による治療では、患者のアドヒアランスに注意する必要があります。 また、インターフェロンフリー治療法の最大の問題点は、ウイルスのゲノムの変異によって起こる耐性獲得の懸念です。 インターフェロンを併用している場合には、ウイルスが耐性を獲得してもインターフェロンによってウイルスを排除することができましたが、これができません。 インターフェロンを含まない2剤併用でウイルス排除に失敗した場合、今後発売される同じ作用機序の薬剤も効かない可能性があります。 野放図な使用による耐性ウイルスの出現が警戒されたことで、適応が限定されました。 【用法・用量】 通常、成人にはダクラタスビルとして1回60mgを1日1回経口投与します。本剤はアスナプレビルと併用し、投与期間は24週間とします。 | ||
| 7. 使用上の注意と服薬支援 | ||
| 【薬剤師への注意】 (1) 本剤はCYP3A4及びP糖蛋白の基質です。また、P糖蛋白、有機アニオントランスポーター(OATP)1B1,1B3及び乳癌耐性蛋白(BCRP)の阻害作用を有します。 よって、以下の併用禁忌薬に注意してください。 リファンピシン,リファブチン,フェニトイン,カルバマゼピン,フェノバルビタール,デキサメタゾン全身投与,セイヨウオトギリソウ含有食品。 また、併用するスンベプラカプセルの禁忌薬にも注意してください。 【患者さんへの説明例】 (1) ダクルインザ錠、スンベプラカプセルは、C型慢性肝炎の治療に用いる抗ウイルス剤です。 2剤を併せて服用することで、ウイルスが増える時に必要なタンパク質に直接作用し、ウイルス排除を目指します。 (2) ダクルインザ錠・スンベプラカプセル併用療法による治療を6ヵ月間受けていただきます。 治療終了6ヵ月後に、血液中にC型肝炎ウイルスが認められるかを確認します。 | ||
| 8. 製造販売元など | ||
| 製造販売元:ブリストル・マイヤーズ株式会社 お問合せ先:ブリストル・マイヤーズ株式会社 メディカル情報部 0120-093-507 |
(文責 下平秀夫) 2014年9月/2015年12月更新