◆ 新薬情報 index
2019年9月製造販売承認
(印刷用画面へ)■フィアスプ注フレックスタッチ,注ペンフィ… ■リティンパ耳科用250μgセット ■アレジオンLX点眼液0.1% ■ラスビック錠75mg ■トリンテリックス錠10mg、20mg ■ハルロピテープ8mg,16mg,24mg… ■コララン錠2.5mg,5mg,7.5mg
■ アレジオンLX点眼液0.1%
|
| 1. 承認概要 | ||
| 新有効成分 2019年9月 / 2019年11月 発売 | ||
| 2. 薬効分類名 | ||
| 抗アレルギー点眼剤 | ||
| 3. 一般的名称 | ||
| エピナスチン塩酸塩 | ||
| 4. 適応症 | ||
| アレルギー性結膜炎 | ||
| 5. 類薬との比較 | ||
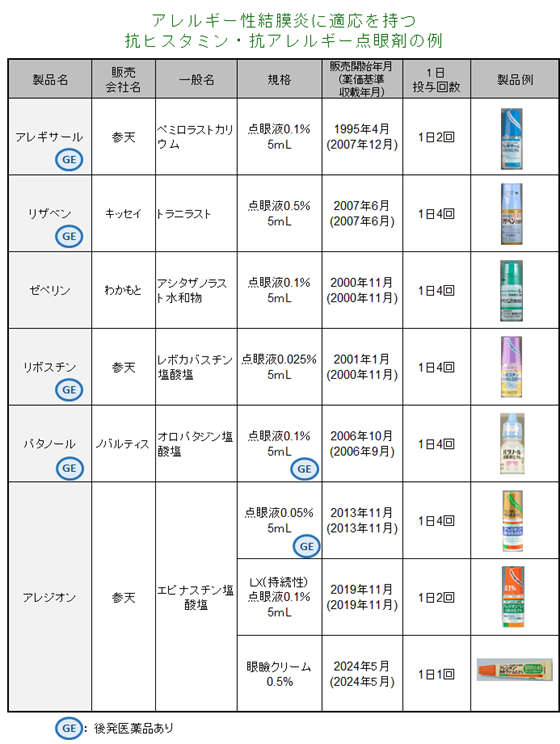 | ||
| 6. 特徴 | ||
| 【特徴】 本剤は、薬剤を高濃度化したことで抗アレルギー作用が長時間持続する1日2回点眼の薬剤であり、アレルギー性結膜炎患者のアドヒアランスと治療満足度の向上が期待できます。 【承認状況】 エピナスチン塩酸塩を0.05%含有する点眼液は、アメリカ、イギリス、フランスなど世界50ヵ国以上で承認されています(2019年5月現在)。日本においても「アレジオン®点眼液0.05%」として、「アレルギー性結膜炎」の効能・効果で販売されています。 【作用機序】 本剤の有効成分であるエピナスチン塩酸塩は、ヒスタミンH1受容体に結合して抗ヒスタミン作用を発揮するとともに、ヒスタミン等のメディエーター遊離抑制作用によりアレルギー性結膜炎に対して治療効果を発揮します。 【用法・用量】 通常、1回1滴、1日2回(朝、夕)点眼します。 【副作用】 本剤の臨床試験で安全性解析対象となった総症例189例において、本剤との因果関係が否定できない臨床検査値異常変動を含む副作用として、結膜充血1例(0.5%)が認められました(承認時)。 なお、アレジオン点眼液0.05%で報告されている刺激感、異物感、羞明、眼瞼炎、眼痛、流涙、点状角膜炎、そう痒感、眼脂が、その他の副作用として注意喚起されています。 | ||
| 7. 使用上の注意と服薬支援 | ||
| 【薬剤師への注意】 1.他の点眼剤と併用する際に少なくとも5分間隔を空けてから点眼します。製剤的工夫によって持続化されたものではないので、点眼順序は指定されていません。 【患者さんへの指導例】 1.この薬は、アレルギー症状や炎症を引き起こすヒスタミンの働きを抑えるとともに、炎症を誘発する物質の放出を抑えます。 2.1日2回の点眼でかゆみを減らします。防腐剤が含まれていないので、コンタクトをつけたままでも使用可能です。 3.点眼時に刺激を感じることがあります。症状が強い場合や継続する場合は、医師または薬剤師に相談してください。 4.ほかの点眼薬を併用する場合には、少なくとも5分以上間隔を空けてから点眼してください。 【ここがポイント!】 本剤は、2013年から発売されているアレジオン点眼液0.05%の高用量製剤です。「LX」は、Lasting extendという造語に由来し、持続性を意味しています。薬剤の高濃度化により、持続性を向上させたことで、わが国で初めての1日2回点眼の持続性抗ヒスタミン点眼薬となりました(アレギサール点眼液は抗ヒスタミン作用なし)。 また、防腐剤フリーの点眼薬ということも特徴に挙げられます。アレジオン点眼液0.05%も、防腐剤としてコンタクトレンズへの吸着や角膜上皮障害が問題となる塩化ベンザルコニウムではなく、ホウ酸を使用しています。本剤は、防腐剤フリーでありながら、保存効力試験に適合しているため、開封後28日間は安全に使うことができ、患者さんへの負担が少ない製剤になったと考えられます。 | ||
| 8. 製造販売元など | ||
| 製造販売元:参天製薬株式会社 提 携:日本ベーリンガーインゲルハイム株式会社 お問合せ先:参天製薬株式会社 製品情報センター 0120-921-839 更新: 2024.7.11:アレジオン眼瞼クリーム承認に伴い、表を更新 |
(文責 下平秀夫) 2020年3月/2024年7月更新
