◆ 新薬情報 index
2019年6月製造販売承認
(印刷用画面へ)■アジマイシン点眼液1% ■ロズリートレクカプセル100mg,200… ■ビレーズトリエアロスフィア56吸入 ■ロナセンテープ20mg,30mg,40m… ■イナビル吸入懸濁用160mgセット ■ゾルトファイ配合注フレックスタッチ
■ ロズリートレクカプセル100mg,200mg
|
|
| 1. 承認概要 | ||
| 新有効成分 2019年6月 / 2019年9月 発売 | ||
| 2. 薬効分類名 | ||
| 抗悪性腫瘍剤/チロシンキナーゼ阻害薬 | ||
| 3. 一般的名称 | ||
| エヌトレクチニブ | ||
| 4. 適応症 | ||
| NTRK融合遺伝子陽性の進行・再発の固形癌 | ||
| 5. 類薬との比較 | ||
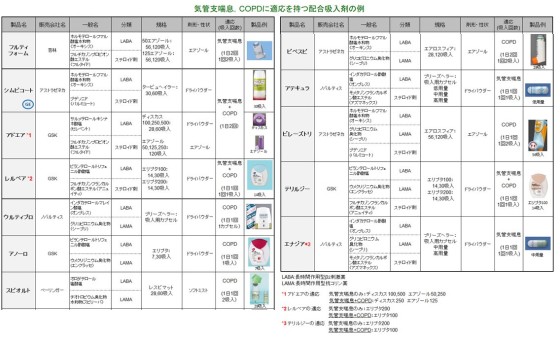 「気管支喘息、COPSに適応を持つ吸入配合剤の例」上の図の、PDFです。2023-05-01更新 | ||
| 6. 特徴 | ||
| 【特徴】 本剤は、小児から成人まで、がん種を問わず横断的に使用できるNTRK融合遺伝子陽性固形がん治療薬として期待されています。 【承認状況】 海外では、本剤が承認されている国または地域はありません(2019年3月時点)。前治療後に疾患が進行または許容可能な標準治療がないNTRK融合遺伝子陽性の局所進行または遠隔転移を有する成人および小児固形がんに対し、2017年5月に米FDAより画期的治療薬(Breakthrough Therapy)に、同年10月に欧EMAよりPRIME(PRIority MEdicines)に指定されています。 【NTRK融合遺伝子】 NTRK融合遺伝子とは、NTRK遺伝子と他の遺伝子が融合してできる異常な遺伝子で、この融合遺伝子から作られるタンパクが発がんの原因になったり、がん細胞の増殖を促進させると考えられています。NTRK融合遺伝子の発生は非常に稀ですが、主要な癌(大腸癌、非小細胞肺癌など)から希少がん(乳腺分泌癌、唾液腺分泌癌、脳腫瘍、軟部肉腫など)、および小児がん(乳児型線維肉腫、中胚葉性腎腫など)まで、様々ながんで確認されています。 【作用機序】 本剤は、ROS1およびTRKキナーゼ活性を阻害することにより、ROS1またはNTRK融合遺伝子を有するがん細胞の増殖を抑制すると考えられています。 【用法・用量】 通常、エヌトレクチニブとして、成人には1日1回600mg、小児には1日1回300mg/m2(体表面積)を経口投与します。用量は600mgを超えない範囲で、患者の状態により適宜減量できます。 【副作用】 多施設共同非盲検国際共同第II相バスケット試験(STARTRK-2試験)において、ロズリートレクが投与されたNTRK融合遺伝子陽性患者63例のうち、57例(90.5%)に副作用が認められました。主な副作用は、味覚異常29例(46.0%)、疲労24例(38.1%)、めまい19例(30.2%)、便秘18例(28.6%)、下痢、浮腫が各17例(各27.0%)、体重増加14例(22.2%)、貧血13例(20.6%)でした。 なお、重大な副作用として、認知障害・運動失調(28.6%)、心臓障害(4.8%)、間質性肺疾患(1.6%)、QT間隔延長(頻度不明)が報告されています(承認時)。 | ||
| 7. 使用上の注意と服薬支援 | ||
| 【薬剤師への注意】 1.妊娠可能な女性患者や、パートナーが妊娠する可能性のある男性患者に投与した場合、妊娠後の胎児への影響が懸念されるため、本剤の投与中および投与終了後、女性30日間、男性90日間は適切な避妊を行う必要があります。 2.心臓障害があらわれることがあるので、この薬の使用前に適宜心機能検査(心電図、心エコーなど)、血液検査などが行われます。 【患者さんへの指導例】 1.この薬は、NTRK融合遺伝子を有するがん細胞の増殖を抑制することで、がんの進行を抑えます。 2.容器を開ける際は、キャップを下に押しながら回して開けてください。 3.グレープフルーツジュースを飲むと、この薬の副作用が強く現れることがあるので、摂取を控えてください。 4.飲み始めてから、息苦しい、むくみや体重の増加、動悸、胸の痛み、倦怠感、発熱、めまいなどの症状が現れた場合は、すぐに医師に連絡してください。 5.自分のいる場所や時間、人の名前がわからなくなったり、いつもできていたことが突然できなくなったりなど、いつもと変わった様子が見られた場合、すぐに受診してください。 【ここがポイント!】 がん治療は、薬剤の開発と同時に遺伝子検査の技術も日々進歩しています。近年では、複数の遺伝子変異を一度に解析できる「がん遺伝子パネル検査」が登場しました。固形がんや肉腫から稀に見つかる異常な遺伝子の1つに、本剤の標的である「NTRK融合遺伝子」があります。この遺伝子の検出については、遺伝子変異解析プログラム「FoundationOne CDxがんゲノムプロファイル」が、本剤のコンパニオン診断として2019年6月に承認されています。 本剤は、厚生労働省より先駆け審査指定制度の対象品目に指定され、2019年6月に世界で初めて承認されました。成人・小児を問わず、NTRK融合遺伝子陽性固形がんへの使用が認められています。 投薬時の対応としては、本剤の服用で発現すると考えられる、貧血、味覚異常、疲労感、吐き気・嘔吐、便秘・下痢、末梢神経障害などの聞き取りが重要です。添付文書には、副作用に対する休薬、減量および中止基準が記載されていますので、疑義照会や処方提案の参考にしましょう。 包装はPTPシートではなく、チャイルドプルーフキャップを採用しているバラ包装なので、開けるときはキャップを下に押しながら回すように説明しましょう。 | ||
| 8. 製造販売元など | ||
| 製造販売元:中外製薬株式会社 お問合せ先:中外製薬株式会社 メディカルインフォメーション部 0120-189706 |
(文責 下平秀夫) 2019年12月/2023年5月更新