◆ 新薬情報 index
2015年7月製造販売承認
(印刷用画面へ)■ランタスXR注ソロスター ■ハーボニー配合錠 ■プラケニル錠200mg ■トルリシティ皮下注0.75mgアテオス/…
■ トルリシティ皮下注0.75mgアテオス/1.5mgアテオス
|
| 1. 承認概要 | ||
| 新有効成分 2015年7月 / 2015年9月 発売 | ||
| 2. 薬効分類名 | ||
| 持効型GLP-1受容体作動剤 | ||
| 3. 一般的名称 | ||
| デュラグルチド(遺伝子組み換え)注射液 | ||
| 4. 適応症 | ||
| 2型糖尿病 | ||
| 5. 類薬との比較 | ||
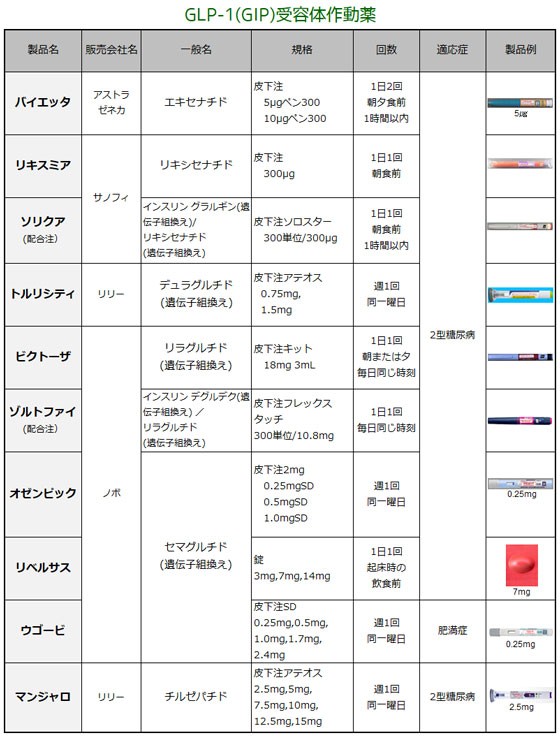 ★ビデュリオン皮下注用2mgペンは2022年5月販売中止。経過措置期間は2023年3月31日で、2023年4月から保険請求はできません。202303更新 | ||
| 6. 特徴 | ||
| 【特徴】 本剤はビデュリオン(一般名:エキセナチド)に続く2剤目の週1回投与のGLP-1受容体作動薬で、2つの特徴があります。 1つ目は、ビデュリオンが23Gと太い注射針であるところ、本剤は29Gと比較的細い注射針であることです。2つ目は、ビデュリオンは投与時に薬剤を懸濁する必要がありますが、本剤は混和が不要となっていることです。 本剤は、1回分の注射液を含むプレフィルドシリンジを注射器に装着したキット製品で、デバイスは「アテオス」という名称です。注射療法の経験がない患者さんの97%が初回から正しく使うことができたということです(海外データより)。 【作用機序】 トルリシティ(一般名:デュラグルチド)は、2つの改変型ヒトGLP-1アナログ領域と改変型ヒト免疫グロブリンG4(IgG4)のFc領域が小型のペプチドリンカーで共有結合した構造の融合糖タンパク質です。 デュラグルチドは他のGLP-1受容体作動薬と同様に、膵β細胞膜上のGタンパク質共役受容体であるGLP-1受容体を介してアデニル酸シクラーゼを活性化させ、膵β細胞内のcAMP濃度を増加させます。その結果、血中グルコース濃度が高い場合にインスリン分泌が促進されます。 【作用時間】 GLP-1受容体作動薬は、その作用持続時間から「短時間作用型」と「長時間作用型」に分けられますが、本剤は「長期間作用型」に分類されます(血中消失半減期が4.5日)。長時間作用型は胃排泄遅延作用が早期に消失するため、悪心や嘔吐の発現は少ないといわれています。 【薬理作用】 デュラグルチドの主な薬理作用は、①グルコース応答性インスリン分泌作用、②グルカゴン分泌抑制作用、③胃内容排出遅延作用で、これらの作用によりグルコース動態とグルコース代謝を調節し、空腹時及び食後血漿中グルコース濃度が低下することで、血糖コントロールを改善します。 【用法・用量】 通常、成人には、デュラグルチド(遺伝子組換え)として、0.75mgを週に1回、皮下注射します。なお、患者の状態に応じて1.5mgを週に1回投与に増量できる。 【アテオスの操作方法】 キャップを外してペンの底面を皮膚に当て、ロックを解除して注入ボタンを押します。 【副作用】 国内臨床試験において、安全性評価対象917例中272例(29.7%)に副作用が認められ、主な副作用は便秘57例(6.2%)、悪心56例(6.1%)、下痢53例(5.8%)でした(承認時)。 その他、重大な副作用として低血糖症状が報告されています。 経口血糖降下薬単剤で血糖コントロール不十分な日本人 2 型糖尿病患者を対象とした試験においてデュ ラグルチド 1.5 mg、週1回投与の有効性及び安全性が確認され2024 年 6 月に承認されました。 | ||
| 7. 使用上の注意と服薬支援 | ||
| 【薬剤師への注意】 (1)糖尿病性ケトアシドーシス、糖尿病性昏睡又は前昏睡、1型糖尿病の患者さんについては、インスリン製剤による速やかな治療が必須となるので、禁忌です。 (2)本剤の適応症では、インスリン製剤やすべての経口血糖降下薬と併用できます。ただし、低血糖リスクが増加するおそれがあることから、SU薬、速効型インスリン分泌促進薬、インスリン製剤を投与中の患者さんで慎重投与となっています。 【患者さんへの説明例】 (1)本剤は1回使い切りの注射剤です。1週間に1回の注射剤で、注入器には1回分の薬液があらかじめ充填されています。1回で全量を使用します。 (2)次回の投与日を忘れないように、カレンダー等に書き留めることをおすすめします。 (3)緑色の注入ボタンを押すと注射が始まり、薬液が自動的に皮膚の下に入っていきます。注入ボタンを押してから薬液が注入され、針が注入器に戻るまでの時間は5~10秒です。注射が完了したら、注射針は注射器の中に自動的に戻ります。 (4)本剤は冷蔵庫(2~8℃)に保管してください。冷蔵庫が使用できない場合、本剤は室温(1~30℃)で14日間まで保管できます。 (5)本剤を凍結させないでください。もし凍結した場合は、使用しないでください。 (6)本剤は高温や直射日光を避けて保管してください。 | ||
| 8. 製造販売元など | ||
| 製造販売元:日本イーライリリー株式会社 販売元:大日本住友製薬株式会社 お問合せ先:日本イーライリリー株式会社 医薬情報問合せ窓口 0120-360-605 大日本住友製薬株式会社 くすり情報センター 0120-034-389 更新:20230330 ビデュリオン皮下注用2mgペンは2022年5月販売中止。経過措置期間は2023年3月31日の件 更新:20240711 トルリシティ皮下注1.5mgアテオス が2024.06に承認されたので追記、表にウゴービ、マンジャロを追加 |
(文責 下平秀夫) 2015年9月/2024年7月更新
