◆ 新薬情報 index
2022年12月製造販売承認
(印刷用画面へ)■ラジカット内用懸濁液2.1% ■アドトラーザ皮下注150mgシリンジ/皮… ■アリドネパッチ27.5mg,同パッチ55…
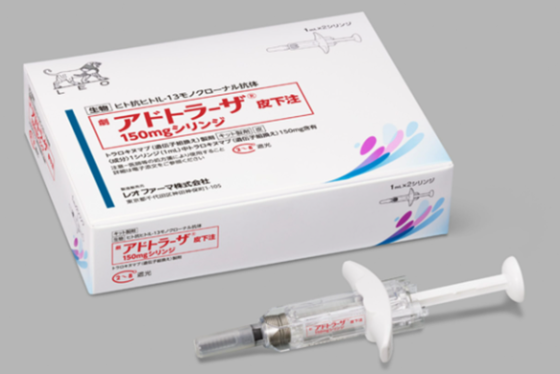
■ アドトラーザ皮下注150mgシリンジ/皮下注300gmペン
|
| 1. 承認概要 | ||
| 新有効成分 2022年12月 / 2023年9月 発売 | ||
| 2. 薬効分類名 | ||
| ヒト抗ヒトIL-13モノクローナル抗体 | ||
| 3. 一般的名称 | ||
| トラロキヌマブ(遺伝子組換え) | ||
| 4. 適応症 | ||
| 既存治療で効果不十分なアトピー性皮膚炎 ■添付文書 ■患者向医薬品ガイド | ||
| 5. 類薬との比較 | ||
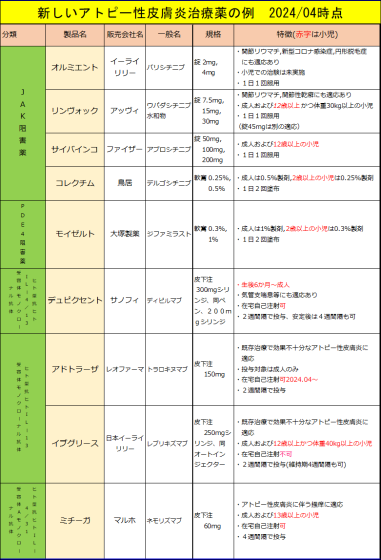 アドトラーザに皮下注300gmペンが追加されています。 | ||
| 6. 特徴 | ||
| 【特徴】 本剤は、アトピー性皮膚炎の増悪に関与するIL-13を特異的に中和するモノクローナル抗体であり、中等症~重症のアトピー性皮膚炎患者の新たな治療選択肢となることが期待されています。 【承認状況】 本剤は、海外ではEU諸国、イギリス、カナダ、アラブ首長国連邦、アメリカ、スイスなど世界21か国で承認を取得しており、中等度~重度のAD療薬として使用されています(2024年12月現在)。 【作用機序】 本剤はヒトIgG4モノクローナル抗体で、2型サイトカインであるIL-13と結合し、IL-13とIL-13Rα1及びIL-13Rα2との相互作用を抑制することでシグナル伝達を阻害し、アトピー性皮膚炎の症状を改善すると考えられています。 【用法・用量】 本剤は、ステロイド外用薬やタクロリムス外用薬などの抗炎症外用薬による適切な治療を一定期間受けても十分な効果が得られず、強い炎症を伴う皮疹が広範囲に及ぶ患者に使用します. 通常、成人にはトラロキヌマブ(遺伝子組換え)として初回に600mgを皮下投与し、その後は1回300mgを2週間隔で皮下投与します。 本剤による治療反応は、通常使い始めてから16週までには効果が得られるため、16週までに効果が得られない場合は投与の中止を検討します。 【副作用】 全身療法が適用となる中等症~重症のアトピー性皮膚炎患者を対象とした臨床試験において、5%以上の頻度で認められた副作用は、上気道感染(上咽頭炎、咽頭炎を含む)、結膜炎、注射部位反応(紅斑、疼痛、腫脹など)でした。 重大な副作用として、重篤な過敏症(頻度不明)が設定されています。
| ||
| 7. 使用上の注意と服薬支援 | ||
| 【薬剤師への注意】 1.2023年3月時点で在宅自己注射は認められていません。 2.本剤は「最適使用推進ガイドライン」の対象医薬品となっています。 【患者さんへの指導例】 1.アトピー性皮膚炎の増悪に関与し、過剰に発現しているインターロイキン-13(IL-13)を特異的に中和するモノクローナル抗体です。 2.この薬を投与中も、症状に応じて保湿外用薬などを併用する必要があります。 3.寒気、ふらつき、汗をかく、発熱、意識の低下などが生じた場合は、すぐに連絡してください。 【ここがポイント!】 本剤は、2024年4月から自己注射可能となりました!! また、これまで、プレフィルドシリンジの150mgシリンジ製剤のみでしたが、2024年12月からオートインジェクターの皮下注300gmペンが発売されて自己注射が簡便になりました。皮下注300gmペンは初回のみ2筒を皮下注します。 本剤は、末梢での炎症を誘導する2型サイトカインであるIL-13を選択的に阻害することで、中等症~重症のアトピー性皮膚炎(AD)に効果を発揮する生物学的製剤です。IL-13は皮膚の炎症反応の増幅、皮膚バリアの破壊、病原体の持続性増強、痒みシグナルの伝達増強などに作用し、IL-13の発現量とADの重症度が相関するとされています。そのため、IL-13を阻害することによって、皮膚のバリア機能を回復させ、炎症や痒み、皮膚肥厚を軽減することが期待されています。 現在、ADの薬物療法としては、ステロイド外用薬およびタクロリムス外用薬(商品名:プロトピックほか)が中心的な治療薬として位置付けられています。近年では、ヤヌスキナーゼ(JAK)阻害作用を有するデルゴシチニブ外用薬(同:コレクチム)、ホスホジエステラーゼ(PDE)4阻害作用を有するジファミラスト外用薬(同:モイゼルト)も発売されました。さらに、これらの外用薬でも効果不十分な場合には、ヒト型抗ヒトIL-4/IL-13受容体モノクローナル抗体のデュピルマブ皮下注(遺伝子組換え)(同:デュピクセント)、ヒト化抗ヒトIL-31受容体Aモノクローナル抗体のネモリズマブ皮下注(遺伝子組換え)(同:ミチーガ)、JAK阻害薬のバリシチニブ錠(同:オルミエント)などが発売され、治療選択肢が広がっています。 本剤は、医療施設において皮下に注射され、原則として本剤投与時もADの病変部位の状態に応じて抗炎症外用薬を併用します。IL-13を阻害することにより2型免疫応答を減弱させ、寄生虫感染に対する生体防御機能を減弱させる恐れがあるため、本剤を投与する前に寄生虫感染の治療を行います。また、本剤投与中の生ワクチンの接種は、安全性が確認されていないため避けます。 臨床効果としては、16週目にEASI75(eczema area and severity index[皮膚炎の重症度指標]が75%改善)を達成した割合は、ステロイド外用薬+プラセボ群では35.7%でしたが、ステロイド外用薬+本剤併用群では56.0%でした。また、32週目のEASI-75達成率は92.5%でした。16週時までのステロイド外用薬の累積使用量はステロイド外用薬+プラセボ群では193.5gでしたが、ステロイド外用薬+本剤併用群では134.9gでした。初期投与期間での主な有害事象はウィルス性上気道感染、結膜炎、頭痛などですが、アナフィラキシーなど重篤な過敏症の可能性があるので十分注意する必要があります。 投与は大腿部や腹部、上腕部に行い、腹部へ投与する場合はへその周りを外し、同一箇所へ繰り返しの注射は避けます。遮光のため本剤は外箱に入れたまま、30℃を超えない場所で保存し、14日間以内に使用します。使用しなかった場合は廃棄します。
| ||
| 8. 製造販売元など | ||
| 製造販売元:レオ ファーマ株式会社 お問合せ先:レオ ファーマ株式会社カスタマーコールセンター 0120-89-0056 更新: 2023.06.18 添付文書へのリンク 更新: 2024.03.26 図に小児適応について加筆 更新: 2024.04.05 本剤が自己注射可能になったことを加筆 更新: 2025.04.01 オートインジェクターの皮下注300gmペンが追加について加筆 |
(文責 下平秀夫) 2023年3月/2025年4月更新