◆ 新薬情報 index
2017年7月製造販売承認
(印刷用画面へ)■ビプレッソ徐放錠50mg,150mg ■アメナリーフ錠200mg ■パルモディア錠0.1mg ■オルミエント錠1mg,2mg,4mg
■ オルミエント錠1mg,2mg,4mg
|
| 1. 承認概要 | ||
| 新有効成分 2017年7月 / 2017年9月 発売 | ||
| 2. 薬効分類名 | ||
| ヤヌスキナーゼ(JAK)阻害剤 | ||
| 3. 一般的名称 | ||
| バリシチニブ | ||
| 4. 適応症 | ||
| 〇既存治療で効果不十分な下記疾患 ・関節リウマチ(関節の構造的損傷の防止を含む) ・アトピー性皮膚炎 ※2020年12月適応追加 ※2024年3月小児適応追加 ・多関節に活動性を有する若年性特発性関節炎 ※2024年3月適応追加 〇SARS-CoV-2による肺炎(ただし、酸素吸入を要する患者に限る) ※2021年4月適応追加 〇円形脱毛症(ただし、脱毛部位が広範囲に及ぶ難治の場合に限る) ※2022年6月適応追加 | ||
| 5. 類薬との比較 | ||
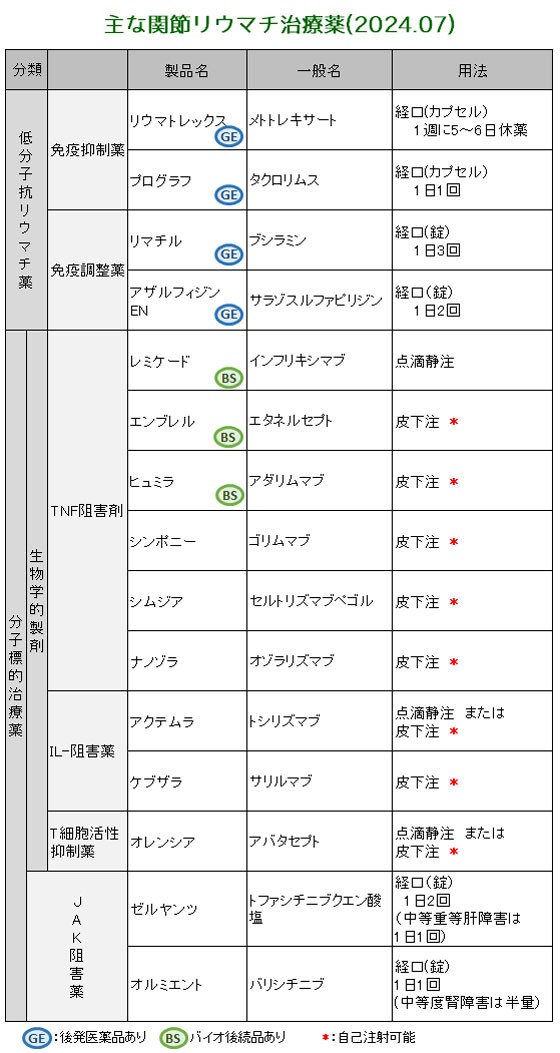 | ||
| 6. 特徴 | ||
| 【特徴】 関節リウマチに用いるJAK阻害薬としてファイザー社のゼルヤンツ錠(成分名:トファシチニブクエン酸塩)に続く2剤目です。ゼルヤンツ錠は通常1日2回ですが、本剤は1日1回経口投与します。経口製剤なので注射部位疼痛によるQOL低下の心配はありません。選択的にJAK1/JAK2を阻害します。 2020年12月に「アトピー性皮膚炎」が適応追加され、2021年4月には「新型コロナ感染症による肺炎」が適応追加されました。続いて2022 年 6 月に「円形脱毛症(ただし、脱毛部位が広範囲に及ぶ難治の場合に限る)」の適応追加が承認されました。さらに、2024 年 3 月に「既存治療で効果不十分な多関節に活動性を有する若年性特発性関節炎」および「小児アトピー性皮膚炎」の適応追加、そして 1 mg 錠の剤形が追加承認されました。 【背景】 関節リウマチ(RA)の薬物療法は近年大きく進展しています。関節破壊の進行抑制を含めた病態コントロールのため、発症初期からメトトレキサート(MTX)を始めとする従来型疾患修飾性抗リウマチ薬(cDMARDs)が使用され、これらの治療で効果不十分な患者に対しては生物学的製剤のTNF阻害薬(エンブレル等)、IL-6阻害薬(アクテムラ等)、T細胞活性抑制薬(オレンシア)、JAK阻害薬(ゼルヤンツ)が使用されています。生物学的製剤は高分子のタンパク質のため内服はできませんが、JAK阻害薬は低分子で消化管で分解されないので、経口投与が可能となっています。 【承認状況】 本剤は2017年7月時点で世界31の国と地域で承認されています。 【作用機序】 JAK阻害薬は、細胞内にあるチロシンキナーゼの一種であるJAK経路を阻害することで複数のサイトカインのシグナル伝達を阻害し、炎症を抑えます。RAの症状発現には IL-6、GM-CSF、IFNγ、IFNα、IL-12 及び IL-23 等の炎症性サイトカインが関与しています。本剤は薬理試験において、IL-6、IFN、IL-12 及び IL-23 等の炎症に関与するサイトカインのシグナル伝達を抑制することが示され、JAK のアデノシン三リン酸(ATP)結合部位に結合し、JAK-STAT 経路を阻害(特にJAK1/JAK2を阻害)することで、炎症や免疫細胞の増殖を抑制すると考えられています。既存薬のトファシチニブ(ゼルヤンツ)は、JAK1、JAK2、JAK3 を阻害し、TYK2 も軽度に阻害しますが、本剤はJAK1、JAK2に高い選択性を有します。 【用法・用量】 〈関節リウマチ、アトピー性皮膚炎(成人)、円形脱毛症の場合〉 通常、成人にはバリシチニブとして4mgを1日1回経口投与します。なお、患者の状態に応じて2mgに減量します。 【臨床効果】 中等度から重度の活動性の関節リウマチ患者を対象とした第 III 相臨床試験において、臨床症状の改善効果、疾患活動性の低下、身体機能障害の改善効果、関節破壊の進展防止効果、患者報告アウトカム(こわばり・倦怠感・痛み)の改善、低疾患活動性及び寛解の達成、及び長期投与時における有効性の維持が認められました。このことから、患者さんのQOL向上が期待されます。また、本剤はトファシチニブと異なり関節破壊防止のエビデンス(mTSS、骨びらんスコア等を比較)があるため、トファシチニブにはない効能効果として「関節の構造的損傷の防止を含む」と記載されています。 【副作用】 JAK阻害薬は生物学的製剤に匹敵する有効性が期待できる経口剤ですが、副作用も類似しており、感染症が多くみられます。重大な副作用として、感染症、消化管穿孔、好中球減少、リンパ球減少、ヘモグロビン減少、肝機能障害、黄疸、間質性肺炎があらわれることがあります。 関節リウマチ患者を対象とした国内外臨床試験(第 II 相及び第 III 相試験)において、本剤が投与された総症例 3439 例中、本剤との因果関係が否定されなかった有害事象は、41.5%に認められました。主な事象は、上気道感染(9.7%)、帯状疱疹(3.9%)等でした。主な臨床検査値異常は、LDLコレステロール上昇(43.2%)等でした。 一方、日本人の関節リウマチ患者を対象に含む臨床試験(第 II 相及び第 III 相試験)において、本剤が投与された総症例 514 例中、本剤との因果関係が否定されなかった有害事象は、68.7%に認められた。主な事象は、上気道感染(24.5%)、帯状疱疹(8.2%)等でした。特に帯状疱疹は、JAK阻害薬に特徴的な副作用です。主な臨床検査値異常は、LDL コレステロール上昇(51.5%)等でした。 【代謝経路】 本剤の主な排泄経路は腎臓ですので、腎機能が低下している患者さんでは排泄が低下します。そのため、eGFR<60の患者さんでは1日1回2mgとしますが、eGFR<30の患者さんには使用しません(禁忌)。 一方、トファシチニブは肝代謝型薬剤であり、重度の肝障害の患者さんには使用できず(禁忌)、またCYP3A4の阻害薬や誘導剤との併用には注意が必要です。 【相互作用】 本剤は主に腎で排泄され、P-糖タンパク、OAT3、MATEの基剤です。OAT3阻害作用を有するプロベネシドとの併用により、本剤のCLr 及び CL/F はそれぞれ 69%及び 51%低下し、本剤のAUCは約2倍に増大しました。プロベネシド等のOAT3阻害作用を有する薬剤との併用時には本剤の服用量は2mg1日1回にします。 | ||
| 7. 使用上の注意と服薬支援 | ||
| 【薬剤師への注意】 (1)免疫反応に関与するJAK経路を阻害するので、感染症の発現や重篤化に注意する必要があります。 (2)過去の治療において、メトトレキサートをはじめとする抗リウマチ薬等による治療を行っても明らかな症状が残る場合に投与します。 (3)ステロイド外用剤やタクロリムス外用剤等による治療で十分な効果が得られない場合に用います。病変部位の状態に応じて抗炎症外用剤、保湿外用剤を継続使用します。(アトピー性皮膚炎) (4)酸素吸入、人工呼吸管理等を要する方を対象に入院下で使用します。(SARS-CoV-2による肺炎) (5)結核の既感染者では、結核に関する十分な問診及び胸部X線検査に加え、インターフェロンγ遊離試験又はツベルクリン反応検査を行い、適宜胸部CT検査等を行う必要があります。 (6)好中球数が500/m㎥未満の患者、リンパ球数が500/m㎥未満の患者、ヘモグロビン値が8g/dL未満の患者さんには禁忌です。 (7)JAK阻害薬は使用前に患者さんに帯状疱疹について注意喚起をする必要があります。 【患者さんへの指導例】 (1)関節リウマチの関節の炎症、腫れや痛みを軽減します。 (2)アトピー性皮膚炎の症状を緩和します。 (3)新型コロナ感染症による肺炎を発症した患者さんの治療において、過剰となっている炎症物質の働きを抑えます。 (4)結核等、重い感染症の方は使用できません。 (5)この薬を服用中にいつもと違う発熱やのどの痛み、息切れ、咳、倦怠感、痛みを伴う発疹や皮膚の違和感などの症状があらわれたらすぐに連絡してください。 | ||
| 8. 製造販売元など | ||
| 製造販売元:日本イーライリリー株式会社 お問合せ先:日本イーライリリー株式会社 Lilly Answers リリーアンサーズ 0120-360-605 【更新】 2024.7.13: 小児アトピー性皮膚炎の適応追加、若年性特発性関節炎の適応追加、錠1mgの剤形追加について加筆 類薬の表にBS製剤追加、ナノゾラ、ケブザラを追加 |
(文責 下平秀夫) 2017年8月/2024年7月更新
