◆ 新薬情報 index
2022年4月製造販売承認
(印刷用画面へ)■ヌバキソビッド筋注
■ ヌバキソビッド筋注
|
| 1. 承認概要 | ||
| 新有効成分 2022年4月 / 2022年5月 発売(薬価未収載) | ||
| 2. 薬効分類名 | ||
| ウイルスワクチン類 生物学的製剤基準 | ||
| 3. 一般的名称 | ||
| 組み換えコロナウイルス(SARS-CoV-2)ワクチン | ||
| 4. 適応症 | ||
| SARS-CoV-2による感染症の予防 | ||
| 5. 類薬との比較 | ||
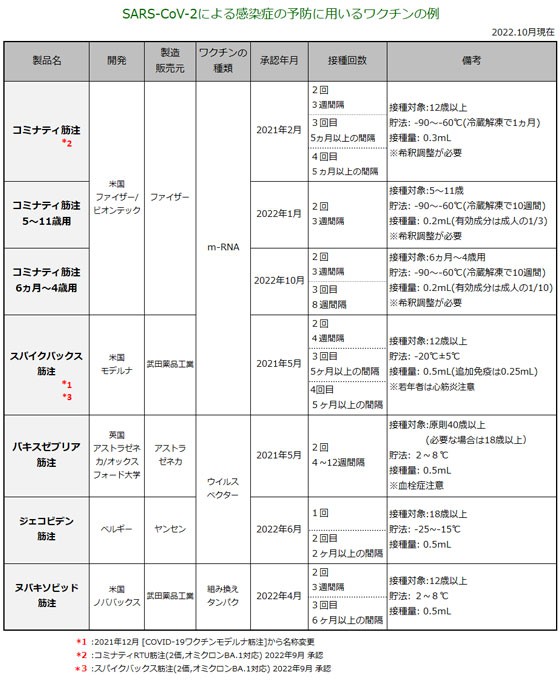 初の「遺伝子組み換えワクチン」です。これまで承認されているワクチンはmRNAワクチン、ウイルスベクターワクチンでしたが、本剤は、初の遺伝子組み換えワクチンでした。 | ||
| 6. 特徴 | ||
| 【特徴】 本剤は、わが国で4番目の新型コロナウイルスワクチンとして承認された国内製造ワクチンです。これまでさまざまな理由により先行3剤の新型コロナワクチン接種が受けられなかった人や3回目接種の新たな選択肢として期待されています。 【承認状況】 40以上の国または地域で条件付き販売承認、または緊急使用許可などとされています(2022年4月現在)。 【作用機序】 本剤は遺伝子組み換えワクチンです。SARS-CoV-2スパイクタンパクの遺伝子を元に、昆虫細胞を用いて発現させた遺伝子組換えSARS-CoV-2スパイクタンパク質をナノ粒子化して製造されたワクチンです。免疫の活性化を促進するためにアジュバント(Matrix-M)が添加されています。本剤の投与により、SARS-CoV-2 のスパイクたん白質に対する B 細胞および T 細胞の免疫応答(中和抗体を含む)が誘導されます。 【用法・用量】 初回免疫 1回0.5mLを2回、通常3週間の間隔をおいて筋肉内に接種します。本剤は2回接種により効果が確認されていることから、原則ほかのSARS-CoV-2に対するワクチンと混同することなく2回接種します。 追加免疫 1回0.5mLを筋肉内に接種します。通常、本剤2回目の接種から少なくとも6ヵ月経過した後に3回目の接種を行うことができます。 【副作用】 臨床試験で報告された主な副反応は、圧痛75.3%、疼痛62.2%、疲労52.9%、筋肉痛51.0%、頭痛49.9%、倦怠感41.0%、関節痛23.9%、悪心・嘔吐14.5%などでした。また、重大な副反応として、ショック、アナフィラキシー(頻度不明)が設定されています。
| ||
| 7. 使用上の注意と服薬支援 | ||
| 【薬剤師への注意】 1.流通に関しては、凍結を避けた2~8℃での保存であり、通常のワクチンと同様に輸送・保管することが可能です。なお、有効期間は9ヵ月とされ、本剤の1バイアルには10回接種分の用量が充填されています。 【患者さんへの指導例】 1.このワクチンを接種することで新型コロナウイルスに対する免疫ができ、新型コロナウイルス感染症(COVID-19)の発症を予防します。 2.医師による問診や検温、診察の結果から接種できるかどうかが判断されます。発熱している人などは本剤の接種を受けることができません。1回目に副反応が現れた場合は、2回目の接種前に医師などに伝えてください。 3.本剤の接種当日は激しい運動を避け、接種部位を清潔に保ってください。接種後は健康状態に留意し、接種部位の異常や体調の変化、高熱、痙攣など普段と違う症状がある場合には、速やかに医師の診察を受けてください。 4.合計2回を3週間の間隔で筋肉内に接種します。1回目の接種から3週間を超えた場合は、できる限り速やかに本剤の2回目の接種を受けてください。 5.初回免疫の2回目接種から少なくとも6ヵ月を経過した人は3回目の接種を受けることができます。 6.本剤の接種直後または接種後に、心因性反応を含む血管迷走神経反射として失神が現れることがあります。接種後一定時間は接種施設で待機し、帰宅後もすぐに医師と連絡を取れるようにしておいてください。 【ここがポイント!】 わが国で4番目の新型コロナワクチンが登場しました。これまで承認されているワクチンはmRNAワクチンであるコミナティ筋注、スパイクバックス筋注と、アデノウイルスベクターワクチンであるバキスゼブリア筋注でしたが、本剤は、初の組み換えスパイクタンパクを抗原とした新型コロナワクチンです。 遺伝子組み換えワクチンはすでにB型肝炎ワクチンなどで実用化されており、一般的に安全性が高く副作用が少ないといわれています。今回、国内臨床試験のデータなどをもとに有効性と安全性が確認され、特例承認ではなく通常承認の枠組みが適用されました。本剤は米国・ノババックスが開発し、わが国では武田薬品工業が技術移管を受けて製造販売と流通を担っています。 本剤には、免疫の活性化を促進するサポニン由来のアジュバントMatrix-Mが添加されており、組み換えスパイクタンパクと組み合わせることで、SARS-CoV-2に対して中和抗体を作るなどB細胞の賦活化およびキラーT細胞などの細胞性免疫の賦活化が誘導されると考えられています。 初回免疫について、米国とメキシコで実施された3万人規模の第III相試験では90.4%、英国で1万5,000人規模の第III相試験では89.7%の発症予防効果が確認されました。 国内の日本人に対する臨床試験でも、海外におけるデータと大きく異ならない結果が得られました。副反応としては疼痛、倦怠感などが確認されましたが、ほとんどが軽度~中等度で、既存の新型コロナウイルスワクチンと比べても特別な懸念はないとされています。 2022年4月27日、厚生労働省の厚生科学審議会予防接種・ワクチン分科会において、本剤を予防接種法に基づく特例臨時接種で使用するワクチンとして、1~3回目接種での使用を想定し、1~2回目接種に用いたワクチンの種類にかかわらず3回目接種への使用が可能となりました。
| ||
| 8. 製造販売元など | ||
| 製造販売元:武田薬品工業株式会社 お問合せ先:武田薬品工業株式会社 くすり相談室 0120-566-587 |
(文責 下平秀夫) 2022年10月